最近,在短短的兩個(gè)月內(nèi),F(xiàn)DA先后批準(zhǔn)了兩個(gè)CAR-T產(chǎn)品上市,像是給本來已經(jīng)熱得發(fā)燙的CAR-T產(chǎn)業(yè)又注射了兩劑強(qiáng)心針。那么,這個(gè)讓無數(shù)病友心動(dòng)、無數(shù)藥企眼饞的CAR-T到底是個(gè)什么東西,它是怎么來的,將來又會(huì)到哪里去?
在這里,我們?cè)噲D通過這篇文章,講清楚CAR-T的來龍去脈,讓淋巴瘤病友們對(duì)CAR-T有一個(gè)全面和清醒的認(rèn)識(shí)。我們將會(huì)提到與CAR-T密切相關(guān)的四位先驅(qū)人物,三家領(lǐng)先企業(yè),兩個(gè)關(guān)鍵專利,和一個(gè)重要問題,相信大家在搞清楚這1,2,3,4之后,對(duì)CAR-T的了解會(huì)比一般的血液科醫(yī)生都要全面(我這么說會(huì)不會(huì)有醫(yī)生來打我?)
在開始之前,先慎重的提醒所有有意參加CAR-T試驗(yàn)的淋巴瘤病友們,目前這個(gè)技術(shù)還處于發(fā)展階段,很多方面還不成熟,實(shí)施過程中也蘊(yùn)含著極大的風(fēng)險(xiǎn),如果不是到了走投無路的地步,還是不要輕易去嘗試這個(gè)東西為好。

圖一:再搶救一下?
一、終極大法
多年以來,人類一直在苦苦探求攻克癌癥的“終極大法”,從手術(shù)到放療再到化療,再到免疫療法,我們已經(jīng)走過了很遠(yuǎn)的路,取得了很大的成就,但是仍然還沒有找到能夠徹底攻克癌癥的“終極大法”。很多人為此付出了畢生的精力,我要說的第一位先驅(qū)人物,就是美國(guó)國(guó)家癌癥研究院(National Cancer Institute,以下簡(jiǎn)稱NCI)外科主任Steven A. Rosenberg,也許很多人都沒有聽說過這個(gè)名字,但是如果我告訴你,當(dāng)初里根總統(tǒng)患結(jié)腸癌的時(shí)候,就是這位老兄給動(dòng)刀切的,這下你該記住了吧?

圖二:NCI外科主任Steven A. Rosenberg
作為一名NCI的外科醫(yī)生,他對(duì)手術(shù)以及放化療在腫瘤治療上的局限性有著深刻的體會(huì)。比如說,轉(zhuǎn)移性惡性黑色素細(xì)胞瘤,手術(shù)不能徹底解決問題,而對(duì)放化療又不敏感,簡(jiǎn)直一點(diǎn)辦法也沒有。可以嘗試用大劑量白介素2來治療,但是有效率充其量不過15%,而且多數(shù)情況下效果不可持續(xù)。Rosenberg就開始動(dòng)腦筋了:腫瘤細(xì)胞附近總是能發(fā)現(xiàn)一些淋巴細(xì)胞,這些細(xì)胞被稱為Tumor Infiltrating Lymphocytes(腫瘤侵潤(rùn)淋巴細(xì)胞,以下簡(jiǎn)稱TIL),從類型來看這些細(xì)胞多為T細(xì)胞,都說T細(xì)胞能夠特異性的識(shí)別腫瘤細(xì)胞抗原,因此是人體抵抗腫瘤的主要武器,那么,能不能利用一下這些T細(xì)胞呢?于是,Rosenberg將惡黑患者腫瘤處的TIL提取出來,和腫瘤細(xì)胞一起做了基因測(cè)序,發(fā)現(xiàn)確實(shí)有一部分T細(xì)胞是由于識(shí)別出了腫瘤細(xì)胞特異性的抗原因此特意跑到腫瘤發(fā)生的部位來進(jìn)行圍剿的,之所以圍剿不成功主要是因?yàn)檫@種細(xì)胞的數(shù)量太少,戰(zhàn)斗力太弱。接下去Rosenberg就做了兩件事,第一是將分離出來的這部分T細(xì)胞進(jìn)行體外擴(kuò)增,極大的增加其數(shù)量,然后再回輸?shù)交颊唧w內(nèi),第二是在回輸完成后分次給患者注射大劑量白介素2。白介素2在這里起什么作用呢?這是因?yàn)門IL屬于已經(jīng)被激活的效應(yīng)性T細(xì)胞,T細(xì)胞被激活后原先位于細(xì)胞表面的低親和性的白介素2受體(IL-2R)會(huì)變成高親和性受體,這個(gè)受體與白介素2結(jié)合后會(huì)使效應(yīng)性T細(xì)胞的殺傷力增大,增殖能力也變得更強(qiáng)。試驗(yàn)的結(jié)果是,這種治療方法的有效率達(dá)到了40%,比以前有了很大的進(jìn)步。后來,這種療法被稱為過繼性細(xì)胞免疫療法(Adoptive Cellular Immunotherapy),過繼性的意思指的是先把細(xì)胞從人體內(nèi)提取出來進(jìn)行培養(yǎng),然后再進(jìn)行回輸。之后發(fā)展起來的LAK細(xì)胞、CIK細(xì)胞、DC-CIK細(xì)胞以及CAR-T細(xì)胞療法都屬于過繼性細(xì)胞免疫療法的范疇,而早年間Rosenberg這個(gè)名字簡(jiǎn)直就是過繼性細(xì)胞免疫療法的代名詞,因此,我們把他稱為是CAR-T療法的前驅(qū)之一,不算過分吧?
但是,在他研究過繼性細(xì)胞免疫療法的年代,基因測(cè)序、體外培養(yǎng)都是既費(fèi)時(shí)又費(fèi)力還費(fèi)錢的事情,幾乎無法在臨床上推廣,只能在實(shí)驗(yàn)室里做研究,所以,臨床上不能說是很成功。另外,從TIL著手,本質(zhì)上講是一種被動(dòng)的手段,因?yàn)樗芯康膼汉谇『檬且环N免疫原性很高的腫瘤(免疫原性指的是抗原刺激機(jī)體產(chǎn)生免疫應(yīng)答的能力),所以他取得了一定的成果,可如果是免疫原性很差的腫瘤,T細(xì)胞根本就識(shí)別不出腫瘤細(xì)胞因而不能做出免疫應(yīng)答怎么辦?
正當(dāng)Rosenberg這位美裔猶太人苦苦思索這個(gè)問題的時(shí)候,他的以色列猶太老鄉(xiāng)卻提前找到了答案,這就是我們所要提到的第二位先驅(qū)人物,即以色列魏茨曼科學(xué)研究院(Weizmann Institute of Science)的科學(xué)家Zelig Eshhar。我不想在這里搞種族主義,但是不得不說猶太人確實(shí)是地球上最聰明的種族之一,一旦他們腦洞大開,整個(gè)世界都會(huì)顫抖,歷史都會(huì)被改寫,如果不服請(qǐng)問問卡爾.馬克思,再問問阿爾伯特.愛因斯坦!

圖三:以色列科學(xué)家Zelig Eshhar
Eshhar和他的同事想到的辦法是:與其說被動(dòng)的等待DC細(xì)胞(樹突狀細(xì)胞)找到腫瘤抗原,將其加工處理后再遞呈給T細(xì)胞讓其識(shí)別,我們?yōu)槭裁床恢鲃?dòng)的給T細(xì)胞裝上一個(gè)能夠識(shí)別腫瘤細(xì)胞特異性抗原的受體呢?恰好,對(duì)逆轉(zhuǎn)錄病毒的研究使得這種想法具有可操作性,因?yàn)槟孓D(zhuǎn)錄病毒這種生物界的奇葩(嚴(yán)格地說病毒甚至不能算是生物)能夠逆天而行用RNA指導(dǎo)DNA的合成,因此是一個(gè)合適的基因?qū)氲妮d體,我們可以用它把想要表達(dá)的基因插入任何一個(gè)細(xì)胞的染色體當(dāng)中。
不過,最初Eshhar的興趣只是在研究MHC限制性上,T細(xì)胞受體(TCR)在識(shí)別靶細(xì)胞例如腫瘤細(xì)胞時(shí),不僅要能夠識(shí)別抗原肽,還要識(shí)別與抗原肽結(jié)合MHC的分子,也就是說必須能夠識(shí)別抗原肽-MHC復(fù)合體,這就叫做T細(xì)胞的MHC限制性,但是腫瘤細(xì)胞為了逃脫免疫監(jiān)視往往會(huì)調(diào)低甚至丟失MHC的表達(dá),這樣T細(xì)胞就無法識(shí)別了,從而失去了作用。
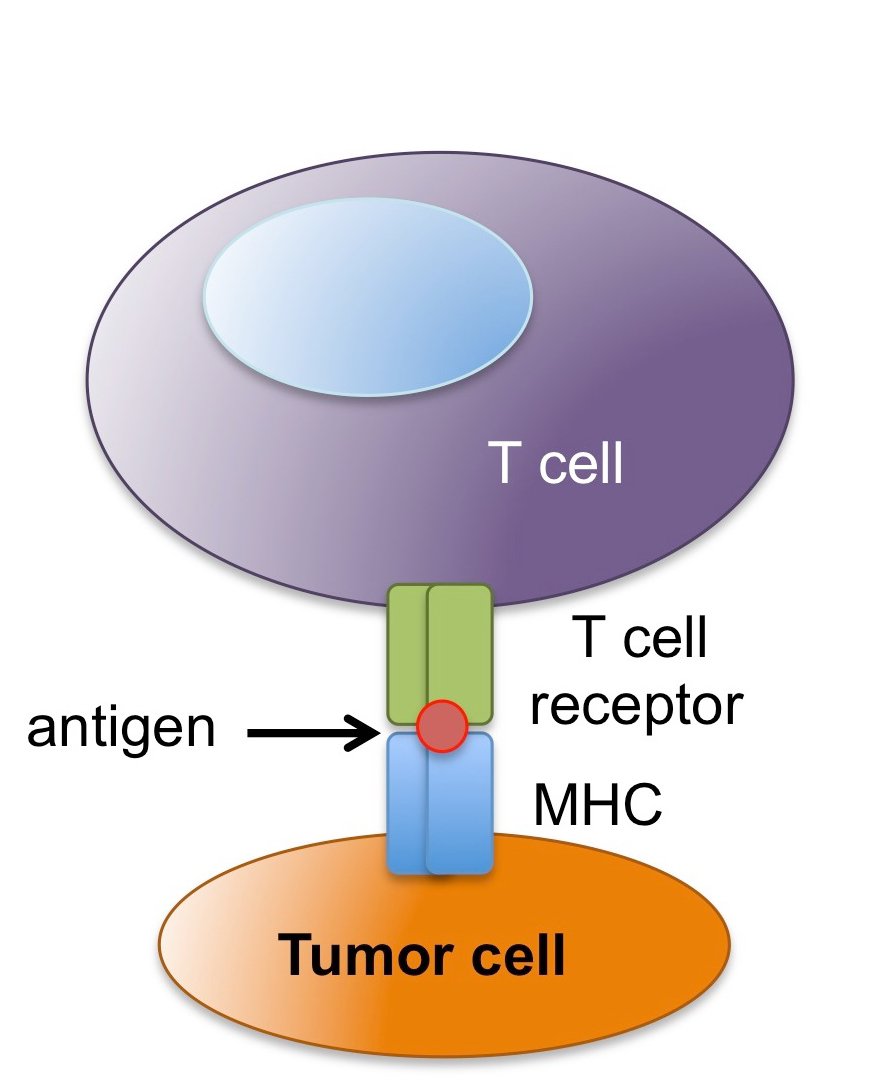
圖四:T細(xì)胞MHC限制性
為了繞開MHC限制性這個(gè)惱人的障礙,Eshhar想出了一個(gè)解決辦法,首先是找到一個(gè)合適的TAA(Tumor Associated Antigen,即腫瘤相關(guān)抗原),然后給T細(xì)胞裝上一個(gè)與這個(gè)抗原相對(duì)應(yīng)的scFv(single chain Variable fragment,即單鏈抗體),嚴(yán)格的說只是抗體的一個(gè)片段,這樣就沒有MHC分子什么事情了,抗原遇到抗體,就像干柴遇到烈火,兩者立刻就開始啪啪啪,于是T細(xì)胞成了裝有制導(dǎo)系統(tǒng)的導(dǎo)彈,想想就覺得很美妙呢,一開始Eshhar將這種經(jīng)過基因修飾的T細(xì)胞叫做T-bodies,這就是CAR-T的雛形。
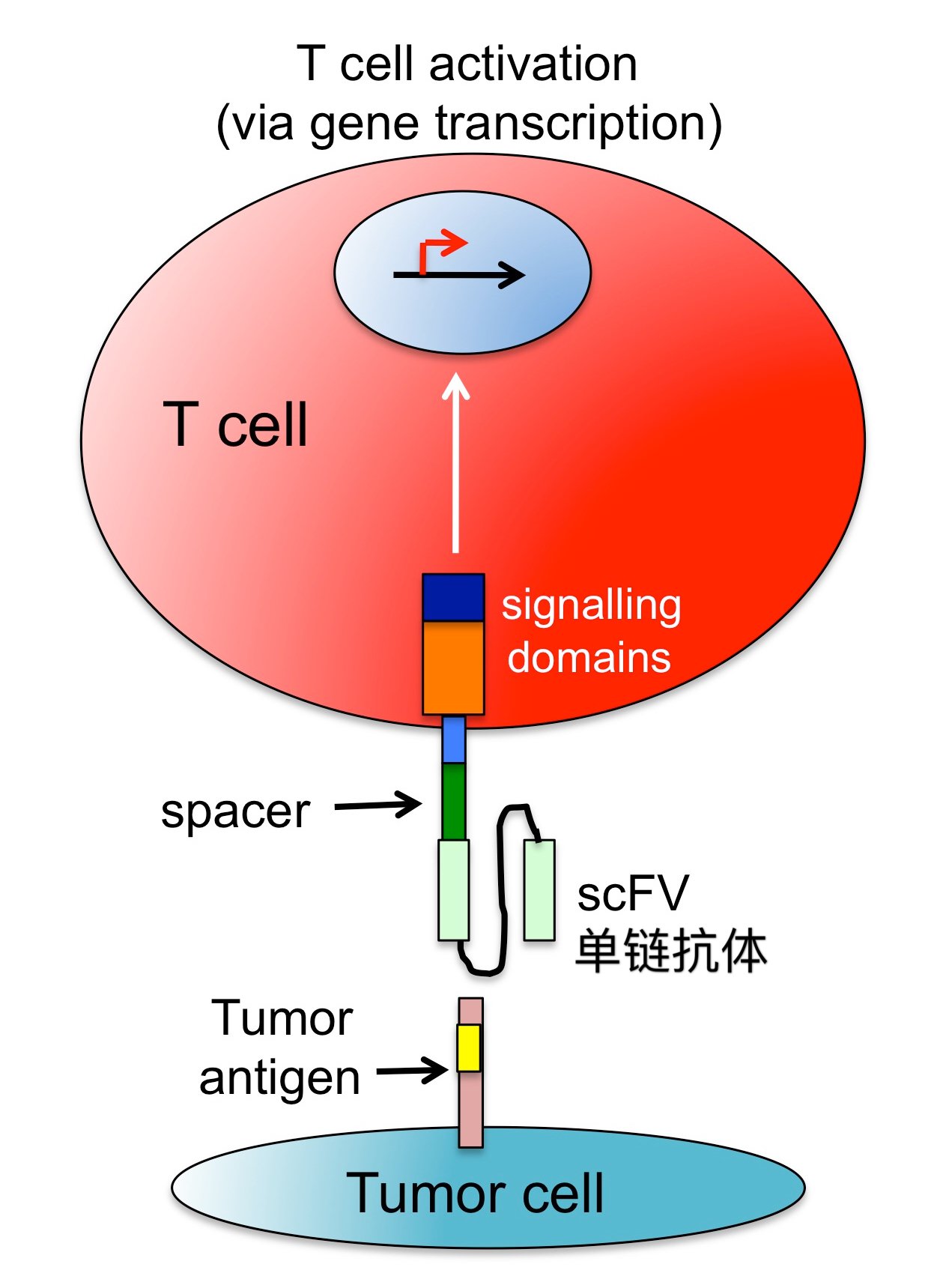
圖五:第一代CAR-T
但是,現(xiàn)實(shí)卻不是想象的那樣美妙,Eshhar的試驗(yàn)多數(shù)時(shí)候都不大成功,首先是很難找到合適的腫瘤相關(guān)抗原,其次,因?yàn)槿狈泊碳ば盘?hào),T細(xì)胞往往會(huì)未老先衰,起不到抗腫瘤的作用。關(guān)于共刺激信號(hào),原理大致如下:T細(xì)胞從胸腺分化成熟然后進(jìn)入外周血時(shí),屬于naive T cell,即初始T細(xì)胞,就好比至尊寶還沒有遇到給他腳底板三顆痣的紫霞,無法變成孫悟空,即成為效應(yīng)性T細(xì)胞,具備殺滅腫瘤細(xì)胞的能力。要激活T細(xì)胞,需要兩個(gè)條件,第一是通過TCR的通路給細(xì)胞核傳送第一個(gè)刺激信號(hào),這是經(jīng)過TCR對(duì)抗原肽-MHC復(fù)合體的識(shí)別實(shí)現(xiàn)的,由CD3的zeta鏈具體實(shí)施,第二個(gè)條件是經(jīng)由CD28-B7通路提供第二個(gè)刺激信號(hào),即T細(xì)胞表面的CD28與樹突狀細(xì)胞或靶細(xì)胞表面的B7結(jié)合從而產(chǎn)生一個(gè)共刺激信號(hào)。造物主這樣的設(shè)計(jì)也是出于無奈,因?yàn)椋约?xì)胞殺傷力太大,如果很輕易的就能激活可能無意中就會(huì)給機(jī)體造成重大傷害。而腫瘤細(xì)胞大多數(shù)情況下并不會(huì)給T細(xì)胞提供B7這個(gè)共刺激分子,因?yàn)樗鼈儾⒉簧?,所以Eshhar的研究進(jìn)展并不順利,直到他給他的T-bodies裝上共刺激分子受體之后情況才有所改觀。所以,可以說以scFv-CDz為基礎(chǔ)的第一代CAR-T基本上是失敗的。
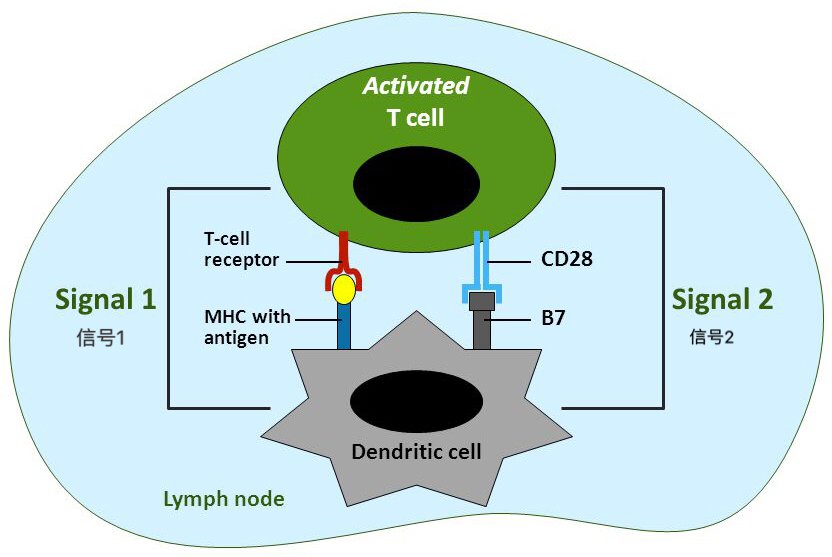
圖六:激活T細(xì)胞需要兩個(gè)信號(hào)
Eshhar只是一名科學(xué)家,不是一名臨床醫(yī)生,將CAR-T發(fā)揚(yáng)光大的重任不應(yīng)該由他來承擔(dān),但是,他確實(shí)對(duì)CAR-T的發(fā)展起到了至關(guān)重要的作用,CAR-T先驅(qū)的稱呼他是當(dāng)之無愧的!
Eshhar等人的研究成果出來后引起了廣泛的關(guān)注,一時(shí)間江湖上風(fēng)起云涌,各路人馬都卯足了勁展開沖刺,要力爭(zhēng)奪下CAR-T的頭一把金交椅,而且,大家不約而同的都把目光從實(shí)體瘤轉(zhuǎn)移到血液腫瘤,特別是B細(xì)胞白血病和淋巴瘤,因?yàn)樽孋AR-T細(xì)胞在實(shí)體瘤上發(fā)揮作用實(shí)在是太難了,而讓T細(xì)胞去對(duì)付B細(xì)胞似乎較為容易。搞科研就像捏柿子,一定要先撿軟的捏,這樣出成果才快,有了成果才會(huì)有投資,有了投資才會(huì)有更多的成果,否則有可能一輩子默默無聞。而最終拔得CAR-T頭籌并且名利雙收的,是我們要介紹的第三位先驅(qū)人物,賓夕法尼亞大學(xué)的Carl H. June和他的團(tuán)隊(duì)。

圖七:賓夕法尼亞大學(xué)的Carl H. June博士
Carl June在做實(shí)習(xí)醫(yī)生的時(shí)候,曾經(jīng)被分配去照看異基因骨髓移植后的患者,那個(gè)時(shí)候移植技術(shù)還很原始,他充分的感受到了T細(xì)胞誘導(dǎo)的排異反應(yīng)對(duì)患者帶來的巨大傷害和可怕后果。后來,他主要從事艾滋病的研究,因?yàn)镠IV病毒主要感染T細(xì)胞,所以對(duì)于T細(xì)胞的研究非常深入,也取得了不少成果。2001年,他的夫人因?yàn)槁殉舶┤ナ懒?,他開始轉(zhuǎn)行搞癌癥研究,一心一意的埋頭苦干,終于在眾多競(jìng)爭(zhēng)對(duì)手中脫穎而出,拿出了有說服力的臨床數(shù)據(jù),他們做出來的針對(duì)B急淋的CTL-019以CD19為靶點(diǎn),用4-1BB做共刺激結(jié)構(gòu)域,屬于第二代CAR-T,獲得FDA批準(zhǔn)后成為全世界第一個(gè)上市CAR-T產(chǎn)品,一時(shí)間Carl June幾乎成了CAR-T代言人,這個(gè)成就應(yīng)該足以讓他告慰夫人的在天之靈了!
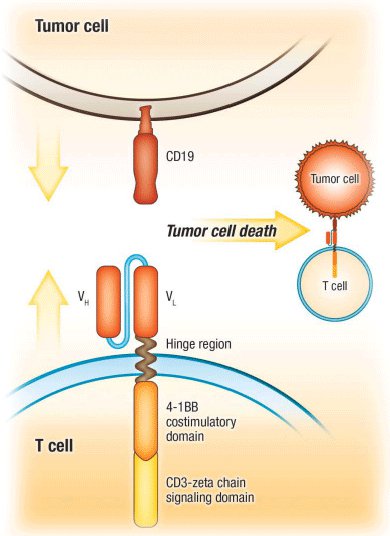
圖八:二代CAR-T產(chǎn)品CTL-019
當(dāng)然,任何的成功其實(shí)都是努力和機(jī)遇的結(jié)合,Carl June的成功離不開另一位我們要介紹的CAR-T先驅(qū)人物,她就是那個(gè)名叫Emily Whitehead的小姑娘。2012年,Emily的急性白血病第二次復(fù)發(fā),醫(yī)生告訴她父母,前面已經(jīng)沒有路可走了,唯一的機(jī)會(huì)是參加臨床試驗(yàn)。恰好,Carl June等人主持的針對(duì)兒童B急淋的CAR-T臨床試驗(yàn)剛剛開始招募患者,之前他們治療了幾位成年患者,但效果一般,但Emily別無選擇,成為了參加這項(xiàng)兒童急性白血病臨床試驗(yàn)的第一位患者。細(xì)胞回輸后沒幾天Emily就進(jìn)了ICU,細(xì)胞因子風(fēng)暴確實(shí)非常可怕,當(dāng)時(shí)醫(yī)生認(rèn)為她只有大約1%的機(jī)會(huì)能挺過來,但是,在醫(yī)生精心的照料下她成功的從ICU中出來了,三周后的檢查未能在她體內(nèi)發(fā)現(xiàn)哪怕是一個(gè)腫瘤細(xì)胞。更為重要的是,她之后沒有做異基因干細(xì)胞移植,而現(xiàn)在已經(jīng)是第五年了,她依然處于完全緩解中,根據(jù)為她提供治療的費(fèi)城兒童醫(yī)院(CHOP)今年7月份的情況更新,她體內(nèi)依然能夠檢測(cè)到CAR-T細(xì)胞,也就是說,可能有一小部分CAR-T細(xì)胞正如所愿的成為了中樞記憶性T細(xì)胞,對(duì)科學(xué)家們來說,這簡(jiǎn)直是美夢(mèng)成真,因?yàn)镃AR-T最理想的效果就是能夠?qū)δ[瘤細(xì)胞起到一個(gè)長(zhǎng)期的監(jiān)視作用,好比打了一個(gè)專門的疫苗,有了抗體以后就終生不會(huì)再犯!

圖九:Emily Whitehead
我們?cè)诖艘仓孕牡淖T高@位名字叫做“愛美麗.白頭”的小姑娘能夠快樂的白頭到老!
毋庸置疑,Emily是至今為止CAR-T技術(shù)最成功的代表人物,是一位明星,但是,她卻并不是第一位從CAR-T中獲益的患者。第一位患者,應(yīng)該是Steven Rosenberg于2010年在《血液》雜志上報(bào)告的一位濾泡性淋巴瘤患者,他先是接受了PACE方案的治療,接著又參加了包括CTLA-4抑制劑在內(nèi)的幾個(gè)臨床試驗(yàn),效果都不好,最后,用了R-EPOCH方案,但也只是部分緩解,Rosenberg給他做了CAR-T治療,靶點(diǎn)是CD19,共刺激分子選擇的是CD28,屬于二代技術(shù),結(jié)果兩次細(xì)胞回輸后,原先的巨大腫塊幾乎完全消失了,雖然沒有實(shí)現(xiàn)完全緩解,但是畢竟算是有史以來CAR-T治療成功的第一個(gè)案例。奇怪的是,Rosenberg的報(bào)告并沒有引起很大反響,也許是因?yàn)橹皇莻€(gè)例,后來人們幾乎忘記了還有這么一位患者。直到2014年,Rosenberg在接受Onclive采訪的時(shí)候,這位患者才再次被提起:

原來,這位患者的疾病五年后仍未出現(xiàn)進(jìn)展,雖然對(duì)于濾泡性淋巴瘤來說不等同于治愈,但是也很了不起吧!所以,我認(rèn)為Rosenberg的貢獻(xiàn)是被under appreciated(低估了),也許他才配得上CAR-T第一人的稱號(hào)。
(二)群雄逐鹿
將一項(xiàng)技術(shù)成果轉(zhuǎn)化為商業(yè)產(chǎn)品,需要有足夠的資源來提供各種保障,重磅抗癌藥品尤為如此。所以,當(dāng)以Carl June為首的賓大團(tuán)隊(duì)被諾華招安的時(shí)候,沒有人覺得奇怪,因?yàn)檫@是順理成章的事情。而諾華這個(gè)制藥巨頭成為全球第一個(gè)成功的摘到CAR-T果實(shí)的公司,即我們所要介紹的第一家擁有領(lǐng)先CAR-T技術(shù)的公司,也是對(duì)他們慧眼識(shí)珠的回報(bào)。特別是當(dāng)Carl June遇到麻煩的時(shí)候,諾華慷慨解囊,成功的化解了危機(jī)。
事情的經(jīng)過是這樣的:各個(gè)科研小組之間,既是競(jìng)爭(zhēng)對(duì)手,也存在合作關(guān)系,因?yàn)殚]門造車是很難有所突破的。Carl June的團(tuán)隊(duì)也一直和其它醫(yī)院的研究人員有合作,比如說,2003年賓大與St. Jude Children’s Research Hospital簽署過一項(xiàng)Material Tranfer Agreement,根據(jù)這項(xiàng)協(xié)議,Carl June的團(tuán)隊(duì)可以與St. Jude的研究人員共享一些研究成果。當(dāng)St.Jude的Dario Campana和Chihaya Imai兩人搞出一個(gè)新的CAR-T細(xì)胞設(shè)計(jì),用4-1BB做共刺激結(jié)構(gòu)域,而不是CD28的時(shí)候,Carl June 要了一份copy,后來大獲成功的CTL-019就是基于這個(gè)設(shè)計(jì)的,然而Carl June在他先后發(fā)表的三篇論文中有意無意的都沒有提到St.Jude以及Dario Campana和Chihaya Imai的名字,于是,St. Jude非常不爽,特別是聽說諾華開始與賓大展開商業(yè)合作的時(shí)候,立刻就向法院提起訴訟。財(cái)大氣粗的諾華,一次性的支付了一千二百多萬美元擺平了這件事情,并且答應(yīng)在產(chǎn)品上市后按比例支付一定的專利費(fèi)。St.Jude的專利,現(xiàn)在歸屬于一家叫做Juno Therapeutics的公司,這也是我們要介紹的第二家在CAR-T技術(shù)上領(lǐng)先的公司,這個(gè)專利,就是我們打算介紹的第一項(xiàng)關(guān)鍵專利,下面我們先說4-1BB是怎么回事。
前面說過,T細(xì)胞被激活需要有一個(gè)共刺激信號(hào),而CD28就是最早被發(fā)現(xiàn)的共刺激分子受體,也是T細(xì)胞上最強(qiáng)的共刺激分子受體,剛發(fā)現(xiàn)時(shí)被稱為clone 9.3,后來被WHO編號(hào)為CD28。CD28的刺激作用有多強(qiáng)呢?國(guó)外曾經(jīng)有一家叫做TeGenro的公司做過一項(xiàng)臨床試驗(yàn),他們搞出一個(gè)CD28的superagonist(超激動(dòng)劑),打算繞過MHC限制性的障礙直接激活T細(xì)胞,結(jié)果成功了,只不過是太成功了,六位年輕健康男性志愿者在注射了這個(gè)CD28超激動(dòng)劑后90分鐘內(nèi)就發(fā)生了細(xì)胞因子風(fēng)暴,12-24小時(shí)內(nèi)就全部進(jìn)了ICU,經(jīng)全力搶救后雖然都活了下來,但是后來這個(gè)公司賠了很大一筆錢,這件事情成為臨床試驗(yàn)歷史上一次慘痛教訓(xùn),打那以后再?zèng)]有人敢輕易的去刺激CD28。
不過,老子在《道德經(jīng)》里說過,“過剛者易折,善柔者不敗”。CD28雖然強(qiáng),但卻不大能夠持續(xù),到了免疫應(yīng)答后期,隨著T細(xì)胞開始表達(dá)CTLA-4等抑制性受體,CD28的表達(dá)就被下調(diào)了,CD28-B7這條信號(hào)通路就不靈光了。所以,T細(xì)胞的持續(xù)活化還需要其它受體的幫忙,其中就包括4-1BB。4-1BB聽上去好像怪怪的,其實(shí)它來源于對(duì)小鼠的gene mapping(基因定位),在小鼠身上編碼這個(gè)受體的基因位于4號(hào)染色體,所以就有了這個(gè)編號(hào),而在人身上對(duì)應(yīng)的基因位于1號(hào)染色體。后來WHO統(tǒng)一編號(hào)的時(shí)候?qū)⑵涿麨镃D137,可見其發(fā)現(xiàn)的時(shí)間遠(yuǎn)比CD28要晚。
4-1BB作為共刺激分子受體雖然不像CD28那么強(qiáng),但是持續(xù)性(persistence)確實(shí)更好,在免疫應(yīng)答后期當(dāng)CD28已經(jīng)衰竭的時(shí)候它仍然表達(dá),也許是出于這個(gè)原因,St. Jude的研究人員將其選做第二代CAR-T細(xì)胞中提供第二信號(hào)的分子。總結(jié)一下,那就是第二代主流的CAR-T產(chǎn)品有兩種設(shè)計(jì),在共刺激結(jié)構(gòu)域,一種用CD28,一種用4-1BB,如果你用4-1BB,就要向Juno買專利授權(quán),got it?
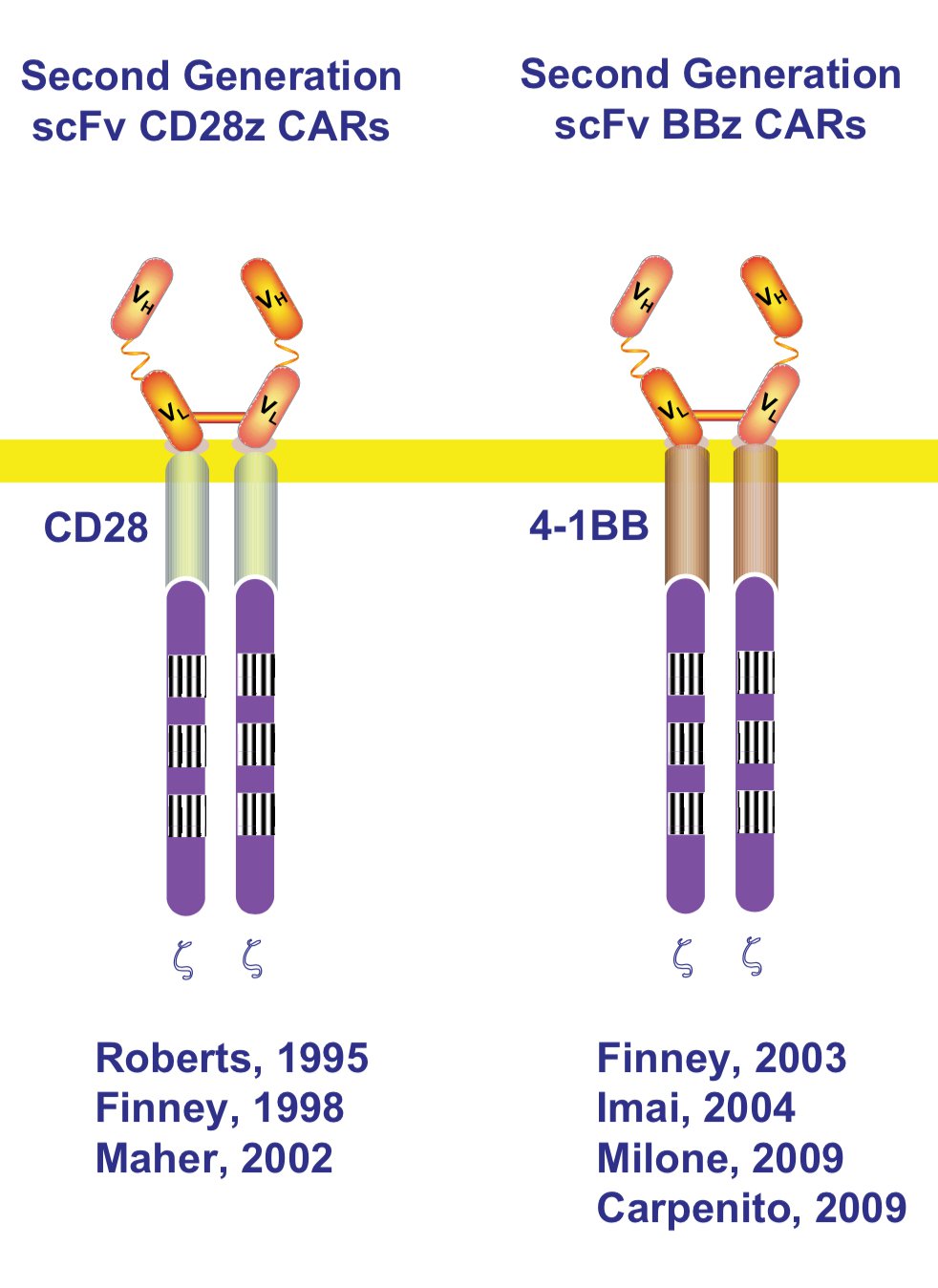
圖十:二代CAR-T的兩種主流設(shè)計(jì)
既然CD28強(qiáng)而不持久,CD137持久但不強(qiáng),那么我們能不能把它們倆結(jié)合在一起,綜合發(fā)揮其各自的優(yōu)勢(shì)呢?當(dāng)然可以,第三代CAR-T就是這么設(shè)計(jì)的:
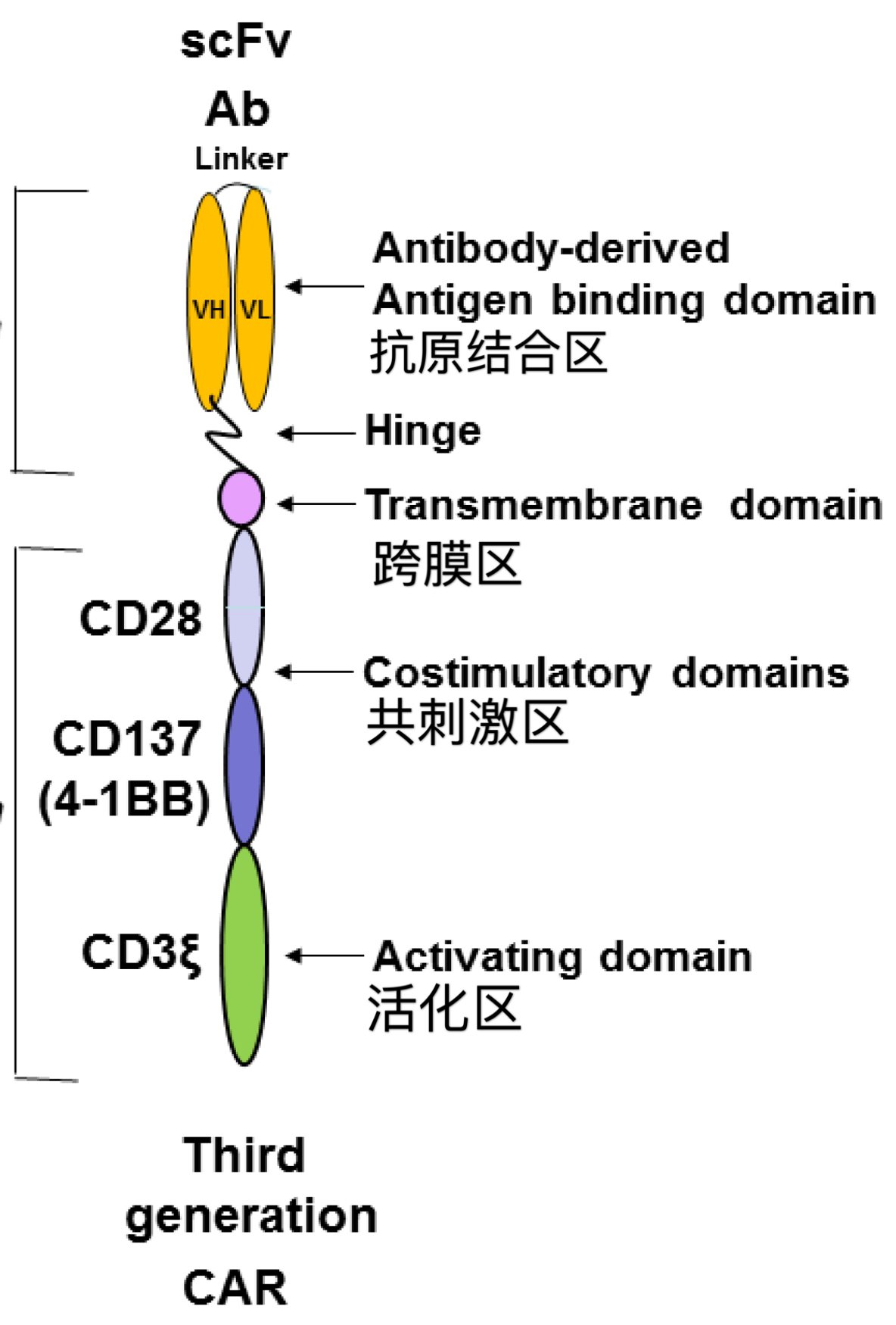
圖十一: 三代CAR-T的設(shè)計(jì)
現(xiàn)在,已經(jīng)有第四代CAR-T,就是在第三代的基礎(chǔ)上再加點(diǎn)什么,比如說讓CAR-T能夠分泌白介素12,進(jìn)一步強(qiáng)化免疫應(yīng)答,或者裝入一個(gè)自殺基因,當(dāng)不良反應(yīng)過強(qiáng)或者未來體內(nèi)的CAR-T細(xì)胞成為麻煩的時(shí)候用藥物讓CAR-T細(xì)胞自我毀滅。由于第四代還沒有公認(rèn)的標(biāo)準(zhǔn)也沒有已經(jīng)成為主流的設(shè)計(jì),下面就不再討論了。而且,目前我們還不敢確信第三代或者第四代一定比第二代更好,所以,準(zhǔn)備參加CAR-T試驗(yàn)的病友不要輕易的被忽悠,在做選擇的時(shí)候不要把第幾代當(dāng)作很重要的考量標(biāo)準(zhǔn),而更應(yīng)該關(guān)注提供這個(gè)產(chǎn)品的生物公司的資質(zhì)。如果同為二代產(chǎn)品,究竟哪種設(shè)計(jì)更好?目前,有不完全的證據(jù)表明,針對(duì)B急淋,4-1BB的設(shè)計(jì)比CD28的設(shè)計(jì)可能更好一些,CD28的設(shè)計(jì)細(xì)胞因子風(fēng)暴更猛烈,而事后T細(xì)胞的衰竭更迅速,復(fù)發(fā)率較高;而針對(duì)非霍奇金淋巴瘤,兩種設(shè)計(jì)目前難分高下。
以Juno的故事為例:雖然他們掌握了4-1BB的專利,但是他們也同時(shí)在開發(fā)CD28的產(chǎn)品,即針對(duì)B急淋的JCAR015,而且最早拿到了FDA的突破性療法的資格認(rèn)定,大家都以為Juno會(huì)先拔頭籌,但沒想到在試驗(yàn)過程中因?yàn)槟X水腫死掉了三個(gè),被FDA叫停試驗(yàn)。于是Juno趕緊出來道歉,并且說經(jīng)過分析是因?yàn)樵陬A(yù)處理方案中同時(shí)使用了環(huán)磷酰胺和氟達(dá)拉濱的緣故,下一步會(huì)取消氟達(dá)拉濱。但是,試驗(yàn)重新開始后又死了兩個(gè),還是腦水腫,F(xiàn)DA再也坐不住了,無限期叫停了這個(gè)試驗(yàn),而 Juno也知道問題不在于氟達(dá)拉濱,而是整個(gè)產(chǎn)品設(shè)計(jì)都有問題,可能與CD28有關(guān)。最終的結(jié)果是,Juno徹底停掉了JCAR015這條產(chǎn)品線,等于說徹底放棄了CD28,專心致志的去賭4-1BB了,但是,考慮到前后耽誤的時(shí)間、花費(fèi)的金錢和失去的生命,代價(jià)可謂非常沉重,Juno不得不吞下苦果,眼睜睜的看著自己的競(jìng)爭(zhēng)對(duì)手,也就是我們要介紹的第三家CAR-T技術(shù)領(lǐng)先的公司KitePharma繼諾華之后拿到FDA的第二個(gè)上市批準(zhǔn)。
Kite Pharma是由以色列出生的猶太裔美國(guó)人Arie Belldegrun于2009年創(chuàng)立的,他是一位泌尿腫瘤科醫(yī)生。作為一家startup的小公司,Kite最初不特別引人注意。2012年,Kite與NCI簽署了一系列合作協(xié)議,包括CAR-T的開發(fā)和商業(yè)化的協(xié)議。2013年,Kite公布了其針對(duì)彌漫大B細(xì)胞淋巴瘤的KTE-C19的初步成果,開始讓人刮目相看。借助于資本市場(chǎng)對(duì)CAR-T概念的熱炒,2014年Kite在納斯達(dá)克上市,圈了大約一億多美元。同年年底,Kite為KTE-C19向FDA提交了IND申請(qǐng)。今年8月,在FDA批準(zhǔn)其產(chǎn)品上市前夕,吉利德宣布以119億美元收購(gòu)Kite Pharma。至此,Kite給所有人展現(xiàn)了一個(gè)極其完美的屌絲逆襲的故事,每一步都走對(duì)了,運(yùn)氣也特別好,從無人關(guān)注的nobody變成了人人仰視的somebody,為此,Kite要感謝一位貴人,那就是我們最初提到了以色列科學(xué)家Zelig Eshhar,從一開始,Kite就把他聘請(qǐng)為科學(xué)顧問,不僅在技術(shù)上提供指導(dǎo),而且他的那項(xiàng)專利也為Kite的定價(jià)做出了極大的貢獻(xiàn),這就是我們要談到的第二項(xiàng)關(guān)鍵專利,US Patent 7741465,美國(guó)媒體上將其稱為Eshhar專利。
前面說過,第一代CAR-T幾乎是Eshhar及其同事一手搞出來的,雖然因?yàn)闆]有共刺激分子因而效果不好,但它卻是后面各代CAR-T的基礎(chǔ),特別是給T細(xì)胞裝上scFv(單鏈抗體片段),這是具有originality的想法,后面的人誰也繞不過去。CAR-T就好比是一棵果樹,現(xiàn)在已經(jīng)接近成熟,所有人都在搶著摘果子,也包括我們中國(guó)的很多公司,沒準(zhǔn)兒我們說話的功夫就又有一家新公司成立了要去摘果子。但是,Eshhar專利就好比是樹干,如果沒有這個(gè)樹干,連枝葉都不可能存在,何況果子。所以,想要摘果子需要先問問Eshhar同不同意哦。
當(dāng)然,如果你有其它專利,是可以拿來交換的,比如說,Juno的發(fā)起人包括位于紐約的紀(jì)念斯隆凱特琳癌癥中心(MSKCC),而MSKCC硬是把二代CAR-T里面的CD28共刺激分子這個(gè)設(shè)計(jì)給注冊(cè)專利了,為此Kite幾乎氣暈,在法庭上和MSKCC打了一架,說CAR-T里面應(yīng)該有一個(gè)共刺激結(jié)構(gòu)是顯而易見的,地球人都知道,不信你在大街上拉住一位大媽問一下她可能都知道。顯然法官不同意這個(gè)說法,結(jié)果Kite的官司打輸了。所以,現(xiàn)在那些正在搶著去摘果子的公司,一定得自己也有點(diǎn)技術(shù)積累和搞一點(diǎn)創(chuàng)新才成,否則人家會(huì)來上門收稅的,畢竟樹是人家栽的,憑什么讓你免費(fèi)摘果子。之所以還沒來,是因?yàn)樨i一定要養(yǎng)肥了再宰,否則哪里有肉?
(三)任重道遠(yuǎn)
好,到這里我們已經(jīng)講完了四個(gè)人物,三家公司和兩項(xiàng)專利。接下去我們就要回答最關(guān)鍵的一個(gè)問題:CAR-T到底能不能成為克制癌癥的“終極大法”?答案是: No! 目前我們距離全面的成功還有太遠(yuǎn)太遠(yuǎn)的距離。雖然以CD19為靶點(diǎn)的CAR-T療法在B急淋和B細(xì)胞淋巴瘤上取得了很大的突破,但是,我們?nèi)匀徊桓艺fCAR-T是這兩種疾病的終極解決方案,因?yàn)檫€有太多太多的問題有待解決,下面一一道來。
讓我們要從頭說起。為什么做CAR-T選定CD19為靶點(diǎn)?前面說過,找到TAA即腫瘤特異性的抗原非常困難,即使找到,也不能保證所有腫瘤細(xì)胞都表達(dá)這個(gè)抗原。而對(duì)于B細(xì)胞來說,無論是正常的B細(xì)胞,還是變成白血病或淋巴瘤的B細(xì)胞,從祖B細(xì)胞開始,到漿細(xì)胞為止,幾乎都穩(wěn)定的表達(dá)CD19,可以說是一個(gè)非常穩(wěn)定的抗原。另外,人是可以長(zhǎng)期沒有B細(xì)胞的,這種免疫缺陷可以用定期輸丙種免疫球蛋白來彌補(bǔ),所以,既然我們找不到B細(xì)胞白血病/淋巴瘤特異性的抗原,我們用好細(xì)胞壞細(xì)胞都表達(dá)的抗原來代替也行,寧可錯(cuò)殺一千,也不放過一個(gè),這是B細(xì)胞白血病/淋巴瘤的優(yōu)勢(shì),換成T細(xì)胞就不行了,我們一刻也離不開T細(xì)胞,這也是為什么到現(xiàn)在為止還沒有針對(duì)T細(xì)胞的CAR-T的原因。
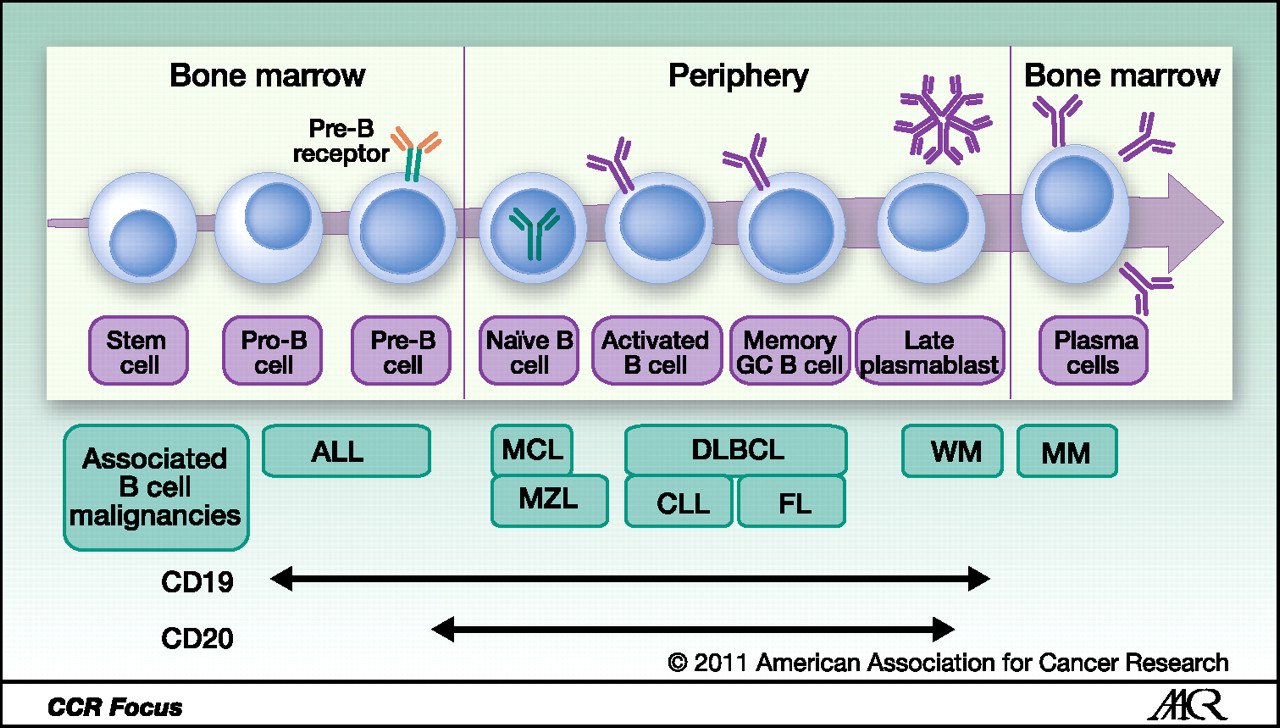
圖十二:CD19在B細(xì)胞中的表達(dá)
那么,既然所有B細(xì)胞淋巴瘤表達(dá)CD19,為什么有人用CAR-T療法完全無效?這也是讓科研人員苦苦思索的問題。主要的原因如下:
1)腫瘤微環(huán)境。腫瘤細(xì)胞不會(huì)是坐以待斃的,通常它們會(huì)分泌一些抑制性的細(xì)胞因子,例如TGF-β和IL-10,其中TGF-β可以抑制T細(xì)胞增殖和降低其細(xì)胞毒性,并且促使T細(xì)胞向Treg細(xì)胞(調(diào)節(jié)性T細(xì)胞)的方向分化;IL-10會(huì)促使單核細(xì)胞分化為M2巨噬細(xì)胞,M2巨噬細(xì)胞表達(dá)PD-L1,對(duì)活化后表達(dá)PD-1的T細(xì)胞有抑制作用;另外,腫瘤細(xì)胞還會(huì)吸引很多Myeloid-derived Suppressor Cells(骨髓來源抑制性細(xì)胞,簡(jiǎn)稱MDSC)到其周邊。Treg細(xì)胞、M2巨噬細(xì)胞和MDSC會(huì)共同形成一個(gè)對(duì)T細(xì)胞極不友好的微環(huán)境,使CAR-T細(xì)胞很難充分發(fā)揮作用。目前,這個(gè)問題主要靠化療預(yù)處理來解決,比如說CAR-T細(xì)胞回輸前做低劑量環(huán)磷酰胺/氟達(dá)拉濱化療,一方面是為了減輕腫瘤負(fù)荷,更重要的是減少體內(nèi)Treg細(xì)胞的數(shù)量,為CAR-T細(xì)胞創(chuàng)造一個(gè)更適合的環(huán)境,這個(gè)環(huán)節(jié)非常重要,也亟待進(jìn)一步優(yōu)化。
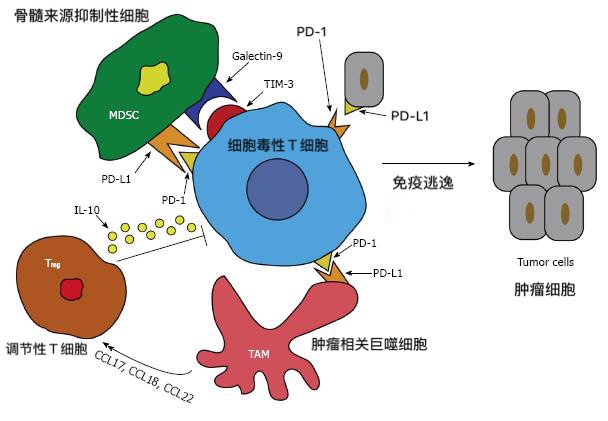
圖十三:抑制性腫瘤細(xì)胞微環(huán)境
2)CAR-T衰竭。在CAR-T治療中,回輸CAR-T細(xì)胞的數(shù)量是有講究的,太多了不行,太少了也不行,我們期待發(fā)生的是CAR-T回輸后會(huì)出現(xiàn)一個(gè)體內(nèi)擴(kuò)增的過程,說明它成功的識(shí)別了靶細(xì)胞并且充分的被激活了。但是由于一些個(gè)體原因,比如患者經(jīng)多次化療后T細(xì)胞質(zhì)量很差,或者腫瘤微環(huán)境中抑制性細(xì)胞因子太多,CAR-T細(xì)胞不能充分的活化和擴(kuò)增而且衰竭很快,就會(huì)使臨床效果大打折扣。
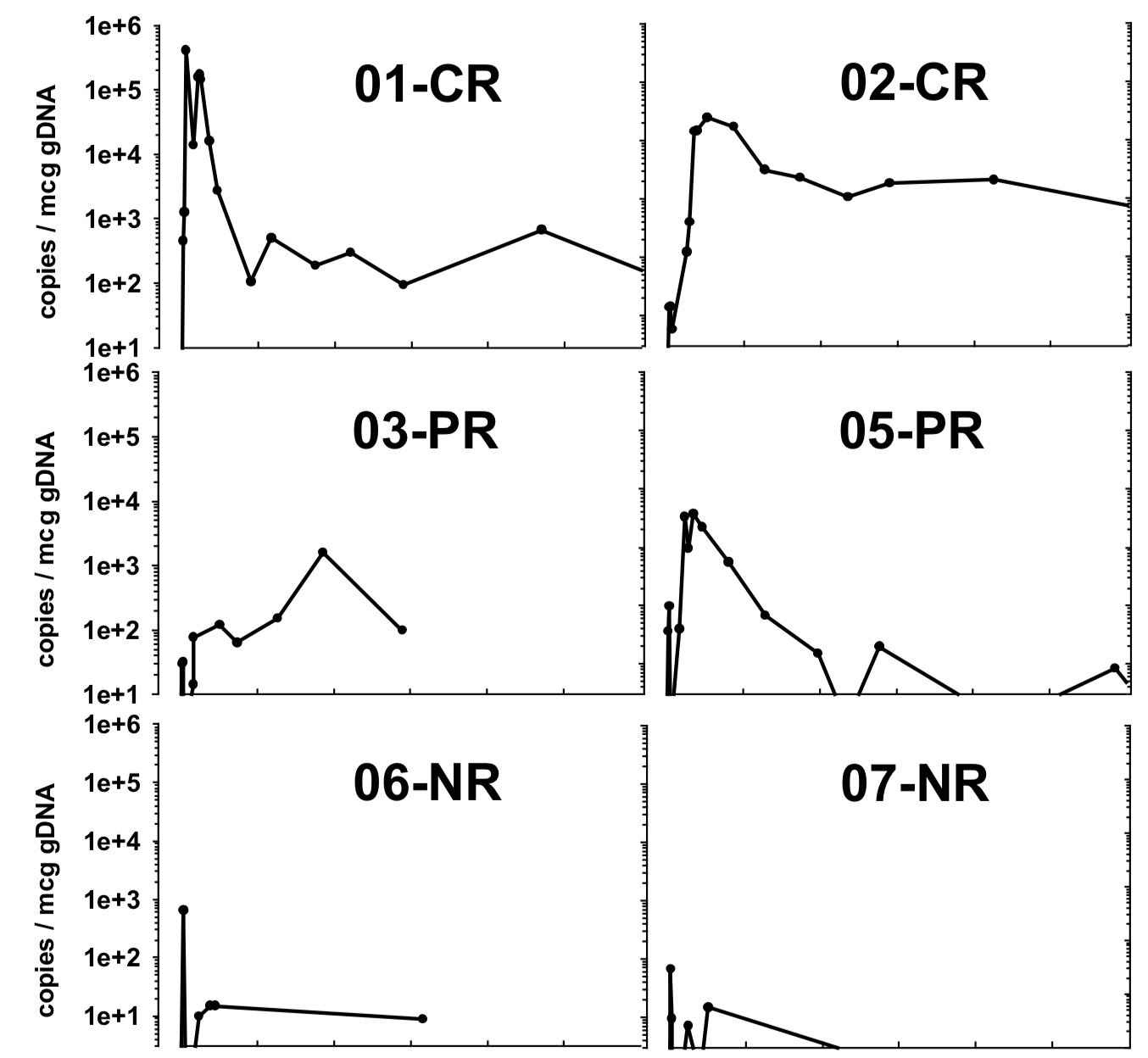
圖十四:CAR-T細(xì)胞回輸后的數(shù)量變化
這是國(guó)外某臨床試驗(yàn)中幾位患者體內(nèi)CAR-T細(xì)胞在回輸后一年內(nèi)的數(shù)量曲線,可以看出,01和02兩位完全緩解的患者CAR-T細(xì)胞先是出現(xiàn)高水平的擴(kuò)增,然后回落但持續(xù)處于較高的水平,而03和05兩位部分緩解的患者CAR-T細(xì)胞數(shù)量衰竭的就比較快,至于對(duì)治療無應(yīng)答的06和07患者,幾乎都沒有出現(xiàn)體內(nèi)擴(kuò)增的現(xiàn)象,CAR-T短時(shí)間內(nèi)就消耗殆盡,難怪沒有效果。所以,現(xiàn)在探究的重點(diǎn)是如何讓CAR-T細(xì)胞在體內(nèi)持續(xù)的更久。
很多患者即使經(jīng)CAR-T治療完全緩解后還會(huì)復(fù)發(fā),這個(gè)怎么破?這是讓研究人員最頭疼的問題。在沒有很好的解決辦法之前,某些情況下就只好把CAR-T僅當(dāng)作通往移植的橋梁,而不是作為獨(dú)立的治愈手段,只求CAR-T能夠在最大程度上降低腫瘤負(fù)荷,為移植創(chuàng)造條件。顯然,這不是一個(gè)讓人非常滿意的解決方案。所以,大家都在研究CAR-T后復(fù)發(fā)的問題,試圖找到更好的辦法。
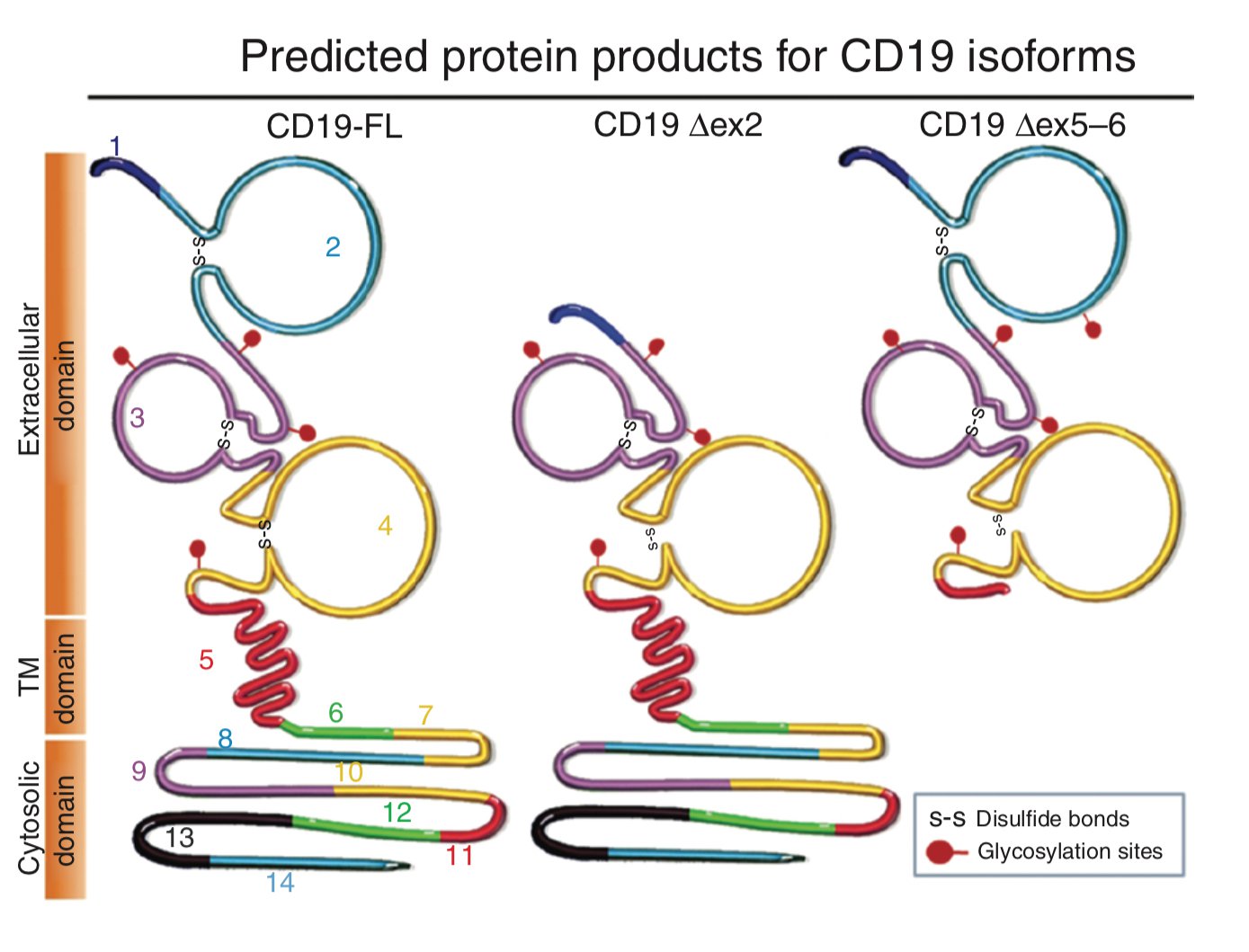
圖十五:基因突變和可變剪切產(chǎn)生不同的CD19蛋白產(chǎn)品
一部分人,復(fù)發(fā)后再次回輸可能還有效,但是大約10%-20%的B急淋和個(gè)別的B細(xì)胞淋巴瘤,復(fù)發(fā)后腫瘤細(xì)胞全部變成了CD19陰性,不再對(duì)以CD19為靶點(diǎn)的CAR-T有應(yīng)答?,F(xiàn)在發(fā)現(xiàn),這是由于兩種原因造成的:1)編碼CD19蛋白的基因2號(hào)外顯子發(fā)生了突變,CD19蛋白丟失了能夠讓抗體識(shí)別的抗原表位;2)5號(hào)和6號(hào)外顯子由于alternative splicing而被剪切掉了,作為一個(gè)跨膜蛋白,其位于細(xì)胞膜內(nèi)的部分因此而丟失,使得整個(gè)蛋白從細(xì)胞上脫落,雖然抗原表位還在,但也沒用了,因?yàn)镃D19已經(jīng)脫離了腫瘤細(xì)胞。有鑒于此,科研人員現(xiàn)在想出了雙靶點(diǎn)的辦法,除了CD19之外,還選擇了CD22這個(gè)B細(xì)胞普遍表達(dá)的抗原作為另一個(gè)靶點(diǎn),并且取得了初步的成功。當(dāng)然,具體的技術(shù)還在優(yōu)化中,到底是應(yīng)該先CD19再CD22,還是CD19/CD22一起來,一起來的時(shí)候把CD19受體和CD22受體裝在同一個(gè)細(xì)胞上還是分別裝在不同細(xì)胞上,目前還沒有答案。
總之,CAR-T技術(shù)還在發(fā)展之中,前途不可限量,但是目前還有太多的不確定因素。
至此,我們就完成了關(guān)于CAR-T的務(wù)虛部分,下篇我們著重于務(wù)實(shí),幫助病友們了解如何從CAR-T療法中獲益。
——摘自《淋巴瘤之家》官網(wǎng)

